Синдром мезенхимальной дисплазии
Синдром мезенхимальной дисплазии
Смысловая нагрузка диагноза «идиопатический сколиоз» означает, что на данном этапе развития медицинской науки этиология заболевания остается неизвестной. Термином «дисплазия соединительной ткани» (ДСТ) называют нарушение формирования соединительной ткани, которое может быть следствием: абнормального синтеза или сборки коллагена; синтеза абнормального коллагена; чрезмерной деградации коллагена; нарушений структуры коллагеновых и эластиновых волокон; разрушения ткани механизмами аутоимунных реакций; влиянием других, пока не изученных механизмов [4]. Диагноз «дисплазия соединительной ткани» ставится на основе тщательного анализа симптомов и результатов клинических исследований. Зачастую сколиоз сопровождают внешние и висцеральные признаки дисплазии соединительной ткани [3]. При этом часто встречаются ситуации, при которых регистрируются различные комбинации признаков ДСТ, наслоение их один на другой, что не позволяет привести полученные данные о пациенте к определенному окончательному диагнозу. Это обстоятельство не противоречит определению понятия синдрома ДСТ, который не является нозологической единицей, а представляет собой генетически детерминированный системный прогредиентный процесс, формирующий фенотипические признаки наследственной патологии и служит фоном при ассоциированных заболеваниях [7].
Недифференцированная ДСТ представляет собой разнородную группу заболеваний, которые, в свою очередь, могут приводить к различным хроническим болезням с нарушениями морфологии и функции внутренних органов [5]. ДСТ характеризуется многообразием клинических проявлений от доброкачественных субклинических форм до полиорганной и полисистемной патологии, нередко с прогрессирующим течением. Клинико-морфологические проявления недифференцированной ДСТ могут включать разнообразные скелетные изменения, связанные с нарушением строения хряща: непропорционально длинные конечности, арахнодактилию, деформации грудной клетки, деформации позвоночника, плоскостопие, патологию развития зубов, прикуса, патологию суставов (склонность к вывихам). Также характерными являются изменения со стороны кожных покровов: гиперэластичность, истончение, склонность к травматизации, внешние признаки ускоренного старения – раннее формирование морщин, деформация овала лица, в том числе и так называемый «гравитационный птоз», клинически проявляющийся обвисанием мягких тканей лица. Кроме того, ДСТ предрасполагает к бронхолегочным и реноваскулярным патологиям, способствует потере мышечной массы (в том числе сердечной, глазодвигательной мускулатуры), что приводит к кардиоваскулярным, офтальмологическим патологиям и нарушениям функции органов желудочно-кишечного тракта [6]. При ДСТ весьма разнообразны поражения сердечно-сосудистой системы: пролапсы клапанов сердца, венозная недостаточность, варикозная болезнь [2; 5].
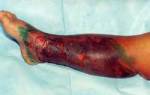
В литературе описана также патологическая кровоточивость, связанная с аномалиями развития соединительной ткани и скелета – геморрагические мезенхимальные дисплазии (ГМД), проявляющиеся сосудистыми, тромбоцитарными и глубокими плазменными нарушениями [1].
Однако проведенный информационный поиск показал, что в исследованиях большинства авторов, посвященных вопросам хирургического лечения идиопатического сколиоза, практически отсутствуют сведения, касающиеся наличия признаков ДСТ у этой категории больных, не уточненной остается частота подобных состояний и степень их влияния на интраоперационную кровоточивость из вынужденно поврежденных тканей.
Цель исследования
- Оценить частоту и характер признаков ДСТ у больных с идиопатическим сколиозом.
- Установить возможную связь фенотипических признаков ДСТ с интраоперационной кровопотерей при хирургической коррекции деформаций позвоночника.
Материал и методы
В исследование включено 99 пациентов подросткового и юношеского возраста с идиопатическим сколиозом, прооперированных в плановом порядке в отделении детской и подростковой вертебрологии Новосибирского НИИТО им. Я.Л. Цивьяна в 2015 г. Учитывая то обстоятельство, что в указанный временной промежуток подавляющее большинство оперированных составили пациенты с идиопатическим сколиозом, больные с более редкими причинами деформаций позвоночника в исследование включены не были.
Собрана и проанализирована информация, включающая: величину деформации позвоночника, возраст больных, объем выполненного хирургического вмешательства, продолжительность операции, тип использованного хирургического инструментария, объем интраоперационной кровопотери, метод анестезиологического обеспечения. Большинство оперированных больных составили дети, подростки и больные юношеского возраста. Средний возраст – 15,7±4,2 года. Величина деформации позвоночника 61,5±19,4°. У всех пациентов на предоперационном этапе оценивалось наличие признаков ДСТ. Во внимание принимались как субъективные (данные анамнеза) критерии, так и данные объективных методов обследования (физикальный осмотр, инструментальные исследования, УЗИ-диагностика).
Для проведения дорсального спондилодеза у всех больных был применен гибридный инструментарий. Все операции выполнялись в условиях одинакового метода анестезиологического обеспечения – общая анестезия на основе севофлурана с ИВЛ. Количество включенных в зону дорсального спондилодеза уровней транспедикулярной фиксации составило 4,2±1,8. Продолжительность хирургического вмешательства – 169,4±30,3 мин. Объем интраоперационной кровопотери – 595,0±200,0 мл.
Статистический анализ полученных результатов выполнен с использованием стандартного пакета программ Microsoft Office 2003 для персональных компьютеров. Стандартная обработка вариационных рядов включала подсчет значений средних арифметических величин (М), стандартных отклонений (m). Сравнение вариационных рядов осуществляли с помощью двухвыборочного критерия Стьюдента (t). Для определения корреляционной зависимости между исследуемыми показателями высчитывался коэффициент корреляции Пирсона (r).
Результаты исследования и их обсуждение
К настоящему времени выделено большое количество фенотипических признаков ДСТ, которые условно разделяются на внешние, выявляемые при физикальном обследовании, и соединительнотканные поражения внутренних органов.
При сборе анамнеза у всех пациентов, включенных в исследование, были выявлены состояния, которые можно рассматривать как косвенные признаки наличия синдрома ДСТ (таблица 1). Большинство обследованных предъявляли жалобы на повышенную утомляемость (49,5%), наличие головокружений (37,4%). При этом у 18% пациентов отмечалось сочетание нескольких патологических состояний. Обращает внимание, что у 12% пациентов ранее наблюдалось состояние повышенной кровоточивости при травмах, экстракции зубов, менструациях.
Мезенхимальная недостаточность, недостаточность соединительной ткани
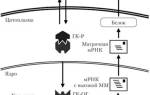
Соединительная ткань — это ткань живого организма отвечающая непосредственно за работу какого-либо органа или системы органов, но играющая вспомогательную роль во всех органах, составляя 60-90 % от их массы. Выполняет опорную, защитную и трофическую функции. Соединительная ткань образует опорный каркас (строму) и наружные покровы (дерму) всех органов. Общими свойствами всех соединительных тканей является происхождение измезинхимы, а также выполнение опорных функций и структурное сходство.
Недостаточность соединительной ткани (синдром дисплазии соединительной ткани) — особенность организма, передающаяся по наследству.
Дисплазийные дети просто находка для тренеров по спортивной и художественной гимнастике, они способны делать чудеса в данной области. В норме почти все суставы нашего организма (кроме позвоночника, тазобедренного и плечевого) двигаются только в сторону сгибания. У этих же детей мы видим переразгибание пальцев рук, коленных и локтевых суставов, чрезмерную гибкость позвоночника. Типичным для проявления этого синдрома является плоскостопие и искривление позвоночника. Именно из таких детей получаются мастера спорта по гимнастике в 11-13лет. Но наши суставы не запрограммированы на такой объем движений, и природа берет свое, через 10-15лет развиваются ранние остеохондроз и остеоартрозы. Таким образом, данная категория детей не должна быть вовлечена в профессиональный спорт.

Видимые, наиболее яркие проявления синдрома дисплазии соединительной ткани (СДСТ) — это проявления со стороны костно-мышечной системы.
Наконец, еще один важный симптом соединительно-тканной недостаточности — нарушение координации работы мелких и крупных сосудов (так называемые ангиотрофо-неврозы).
Если сосуды, состоящие из соединительной ткани, неполноценны, то нейрогормональные механизмы их регуляции тоже работают неслаженно. Так возникают вегето-сосудистая дистония, гипо- и гипертонические болезни, атеросклероз, аневризмы,воспалительные процессы и др. Таким образом, трофика тканей ухудшается, и замыкается порочный круг соединительно-тканной недостаточности.
Огромная роль соединительной ткани в протекании процессов старения организма. Еще Илья Мечников указывал на износ соединительной ткани как на основную причину старения: «Человек стар настолько, насколько стара его соединительная ткань» — писал он.
Заболевания, связанные с недостаточностью соединительной ткани
-
В связи со слабостью связочного аппарата, недостаточной прочностью коллагеновых волокон могут развиваться такие заболевания, как
- Гипермобильность суставов
- Опущение различных органов
- Остеопороз
- Остеохондроз
- Коллагеновая недостаточность
- Недостаточность митрального клапана
- Плоскостопие
- Сколиоз
Методы воздействия на соединительную ткань
-
Единственной системой, способной как-то компенсировать недостаточность соединительной ткани, является мышечная система. Отсюда зависят профилактические рекомендации и лечения данной патологии. В нашем медицинском центре Вам помогут справиться со многими симптомами ее проявления и улучшить качество Вашей жизни.
- Иглорефлексотерапия
- Гирудотерапия
- Мануальная коррекция
- Электрофорез
- Гимнастика Ниши (ЛФК)
- Свинг-терапия
- Подводный ручной массаж, гидромассаж
- Кинезотерапия
Все права защищены законом об авторском праве. Никакая часть содержимого сайта не может быть использована, репродуцирована, передана любым электронным, копировальным или другим способом без предварительного письменного разрешения владельца авторских прав.
Ассоциированная патология у детей с дисплазией соединительной ткани
Опубликовано в журнале:
«ПРАКТИКА ПЕДИАТРА»; №3 (сентябрь-октябрь); 2019; стр. 32-38.
Э. А. Юрьева, д-р мед. наук, проф., главный научный сотрудник лаборатории клинической геномики и биоинформатики, В. С. Сухоруков, д-р мед. наук, проф., кафедра гистологии, эмбриологии и цитологии, Е. С. Воздвиженская, канд. биолог. наук, биолог лаборатории патоморфологии и иммунологии, М. В. Кушнарева, д-р мед. наук, проф., главный научный сотрудник отдела неонатологии и патологии детей раннего возраста, А. Н. Семячкина, д-р мед. наук, проф., главный научный сотрудник отдела клинической генетики, М. Н. Харабадзе, канд. мед. наук, заведующая педиатрическим отделением врожденных и наследственных заболеваний ОСП «НИКИ педиатрии им. акад. Ю. Е. Вельтищева» ФГБОУ ВО РНИМУ им. Н. И. Пирогова
Резюме: Нарушение кислород-транспортной функции эритроцитов в сочетании с хроническим окислительным стрессом обусловливает сердечно-сосудистую патологию и структурно-функциональные нарушения во многих тканях и органах, в первую очередь, в сердечно-сосудистой системе, органах желудочно-кишечного тракта, начиная с полости рта (системная гипоплазия эмали, множественный кариес, хронический гингивит), отмечается дисфункция билиарного тракта, гастродуоденит. Характерные аномалии органов мочевой системы и сосудистая патология сопровождаются возникновением и хронизацией симптомов дисметаболической нефропатии (никтурия, микропротеинурия, тубулоинтерстициальный нефрит, кальциноз почек). Нередкие артериальные мальформации в легких сопровождаются бронхитами, в том числе аллергической природы (IgE). Костная патология включает остеопороз, сколиоз, переломы. Представленные данные свидетельствуют о нарастании частоты тяжести сопутствующих заболеваний с возрастом, отличающихся большей тяжестью течения при синдроме Марфана.
Ключевые слова: дисфункция соединительной ткани, ассоциированные болезни, гипоксия, дети
Summary: Violation of the oxygen-transport function of erythrocytes in combination with chronic oxidative stress causes cardiovascular pathology and structural and functional disorders in many tissues and organs, first of all, in the cardiovascular system, organs of the gastrointestinal tract, starting from the oral cavity (systemic enamel hypoplasia, multiple caries, chronic gingivitis); dysfunction of the biliary tract, gastroduodenitis are noted. Typical abnormalities of the urinary system and vascular pathology are accompanied by the onset and chronicity of symptoms of dysmetabolic nephropathy (nocturia, microproteinuria, tubulointerstitial nephritis, kidney calcification). Frequent arterial malformations in the lungs are accompanied by bronchitis, including those of an allergic nature (IgE). Bone pathology includes osteoporosis, scoliosis, fractures. The data presented indicate an increase in the incidence of severe concomitant diseases with age, which are more severe with Marfan syndrome.
Keywords: connective tissue dysfunction, associated diseases, hypoxia, children
Состояние организма при наследственных хронически протекающих болезнях у детей в значительной степени зависит от адекватной и своевременной компенсации возникающих нарушений функций органов и систем. Главное значение, несомненно, отводится гипоксии, которая проявляется у детей с наследственными болезнями соединительной ткани, в частности, при синдромах Элерса-Данлоса и Марфана уже во внутриутробном периоде [ 1 ] — [3]. Недостаток кислорода может быть вызван не только внешними, но и внутренними факторами, к которым относятся нарушения кровообращения как центрального, так и периферического, наличие легочной и сердечной недостаточности, токсикоз. В таких случаях в крови значительно снижается газообмен, нарушается транспортировка кислорода к тканям (гемическая гипоксия). Тканевая гипоксия развивается из-за снижения способности гемоглобина отдавать кислород тканям или из-за снижения способности тканей экстрагировать кислород. Хроническое течение гипоксии вызывает необратимые изменения в органах, нарушая их работу и формируя с годами многие вторичные заболевания. Как компенсаторная реакция в крови возникает характерное увеличение содержания эритроцитов и гемоглобина [3]—[11]. Среди клинических симптомов кислородного голодания наиболее частыми являются постоянная усталость, низкая толерантность к физическим нагрузкам, бледность кожных покровов, мышечная гипотония, быстрая утомляемость, головная боль [12].
Цель работы – установить взаимосвязь изменения отдельных показателей дисметаболизма при ассоциированной патологии с клиническими симптомами кислородной недостаточности у детей с наследственной дисплазией соединительной ткани.
Материалы и методы. Под наблюдением находились три группы детей: 2 группы с синдромом Элерса-Данлоса, из которых в первую группу были включены дети в дошкольном возрасте (20 человек) а во вторую – дети школьного возраста (20 чел.), в третью группу вошли дети с синдромом Марфана (10 чел.), в возрасте от 5 до 17 лет, при обоих синдромах преобладали мальчики (1,6 : 1).
Функциональные методы включали ЭКГ, реоэнцефалограмму, ЭХО-КГ, УЗИ брюшной полости, почек, щитовидной железы, дуплексное сканирование сосудов шеи, рентгенограммы костей кистей, предплечий, голеней и коленных суставов, денситометрию костей. Проводились консультации специалистов: генетика, педиатра, невролога, нефролога, кардиолога, психолога, эндокринолога, гастроэнтеролога, хирурга, ортопеда, отоларинголога, офтальмолога и других по показаниям. Проводился общий и биохимический анализ крови, включая исследование гормонального, иммунного статуса; общий и биохимический анализ мочи, анализ мочи по Зимницкому, по Ничипоренко, исследовался газовый состав крови. Полученные результаты подвергались статистической обработке с помощью компьютерных программ Microsoft Word определения парных корреляций с применением метода вариационной статистики.
Клинический симптомокомплекс у наблюдаемых больных с наследственными заболеваниями соединительной ткани свидетельствовал о хроническом нарушении кислородного статуса организма. У всех детей отмечались быстрая утомляемость, слабость, низкая толерантность к физическим нагрузкам, головная боль, гипотония мышечной ткани, нарушения физического развития. Обращал на себя внимание мультисистемный характер клинических симптомов вовлечения в патологический процесс различных органов и тканей. Основой снижения способности поддерживать в норме кислородный статус явились дегенеративные изменения соединительной ткани, обусловленные нарушением синтеза коллагена (синдром Элерса-Данлоса), или гликопротеина внеклеточного матрикса -фибриллина (синдром Марфана). В обоих случаях у больных детей выявлялись более или менее тяжелые нарушения функции сердца и сосудов, органов дыхания, опорно-двигательного аппарата, зрения, стоматологического статуса. Аномалии сердца и сосудов в свою очередь обусловливают высокий риск сердечной недостаточности как в покое, так и при нагрузке, ухудшают способность сердца к наполнению и опорожнению, обусловленные повреждением миокарда, создают угрозу развития диффузных обменных нарушений [13]-[16]. Результаты лабораторных исследований представлены в табл. 1. Несмотря на клинический полиморфизм патологических проявлений у детей всех трех групп, обращает на себя внимание устойчивое повышение количества эритроцитов независимо от значительной разницы в содержании гемоглобина, особенно в 1-й и 3-й группах по сравнению со 2-й группой.
Таблица 1.
Биохимические показатели крови и мочи у детей с синдромами Элерса-Данлоса и Марфана (в зависимости от возраста)
Підвищуйте свій
професіоналізм
УЛЬТРАЗВУКОВАЯ ДИАГНОСТИКА РЕДКОЙ ПАТОЛОГИИ ПЛАЦЕНТЫ: ПЛАЦЕНТАРНАЯ МЕЗЕНХИМАЛЬНАЯ ДИСПЛАЗИЯ
Национальная медицинская академия последипломного образования имени П.Л.Шупика, г.Киев
Введение. Плацентарная мезенхимальная дисплазия (ПМД), также известная как мезенхимальная стволовая ворсинчатая гиперплазия, является редкой плацентарно-сосудистой аномалией, эхографически характеризующаяся плацентомегалией и множественными гроздьеподобными кистозными полостями, напоминающими пузырный занос.
Цель: представить эхосемиотику плацентарной мезенхимальной дисплазии, обсудить дифференциально-диагностический ряд и прогноз беременности.
Материалы и методы: представлен случай ПМД, диагностированный во втором триместре с нормальным исходом беременности.
Результаты и обсуждение. 33-х летняя беременная была направлена на консультативное УЗ исследование в 19 недель беременности в связи с подозрением на крупную хориангиому плаценты. Настоящая беременность вторая, первая закончилась рождением здорового ребенка. Клиническое течение настоящей беременности без особенностей. При УЗИ размеры и анатомия плода соответствовали сроку беременности. Плацента располагалась на задней стенке матки. Интраплацентарно определялся крупный участок кистозно измененной плаценты, выбухающий в амниотическую полость, размерами 80х60 мм. Измененный участок паренхимы плаценты был представлен множественными кистозными полостями, напоминающими «соты», приблизительно одинаковых размеров, диффузно расположенными на всем протяжении от хориальной до базальной пластины. Зона поражения имела четкое отграничение от нормально сформированной плацентарной ткани. В отличие от хориоангиомы, в режимах ЦДК в зоне поражения определялись единичные низкоскоростные венозные сосудистые сигналы. Отсутствовали особенности цветового картирования сосудов базальной и хориальной пластин. Пуповина прикреплялась вблизи зоны поражения. На остальном протяжении плацентарная ткань имела обычное эхографическое отображение. Биохимические показатели, в т.ч. уровни АФП и ХГЧ были нормальными. В динамике наблюдения в сроки 24 и 28 недель данный участок не изменялся, рост плода соответствовал долженствующему. В 33 недели впервые отмечены участки варикозного расширения сосудов хориальной пластины с венозным спектром кровотока. Последнее УЗИ выполнено в сроке 35 недель. Результаты мультиваскулярного допплеровского мониторинга не выявили отклонений в гемодинамике фетоплацентарного комплекса на протяжении всего периода наблюдения. В связи с выявленными варикозно расширенными сосудами и близким расположением места прикрепления пуповины было принято решение в пользу планового кесарева сечения, выполненного на 40-й неделе. Родилась доношенная девочка массой 3560г, рост 53см. Оценка по Апгар 8-9 баллов. Макроскопически:плацента увеличена, с варикозным расширением вен хориальной пластины, в плацентарной паренхиме определялась зона множественных кистозных полостей (напоминают гроздья винограда, как и при пузырном заносе). Микроскопически: среди нормальной плацентарной ткани выявляются поля, состоящие из увеличенных стволовых ворсин с цистерноподобными образованиями, хорангиоматозные измененения ворсин. Пролиферация трофобласта и трофобластические включения, патогномоничные для частичного пузырного заноса отсутствовали.
Прогноз исхода беременности по данным литературы неопределенный. Наиболее частым осложнением беременности при ПМД является ЗРП, скорее всего связанная с шунтированием крови плода в сосудистые мальформации или тромбозом кровеносных сосудов стволовых ворсин, что приводит к гипоперфузии и гипоксии. Также отмечена высокая частота преждевременных родов. Материнские осложнения встречаются редко и вряд ли имеют прямую связь с ПМД. По-видимому, исход беременности скорее определяется относительным размером и ростом функционально полноценной плаценты, а не наличием ПМД. В связи с этим требуется динамический мультиваскулярный допплеровский мониторинг функционального состояния фетоплацентарного комплекса. Необходима тщательная оценка анатомических структур плода для исключения фетальных аномалий, в частности синдрома Беквита-Видемана, опухолей печени. В сомнительных случаях показана инвазивная пренатальная диагностика.
Дифференциальную диагностику ПМД, в первую очередь, следует проводить с частичным пузырным заносом, полным пузырным заносом при бихориальной двойне с нормальным вторым плодом, поскольку утолщенная плацента с множественными анэхогенными полостями являются классическими эхографическими находками как ПМД, так и пузырного заноса. При фокальном поражении (как в нашем случае) ПМД может потребоваться дифференциальная диагностика с хориангиомой . субхориальной гематомой, плацентарной кистой, идиопатической аневризматической дилатацией субхориальных сосудов.
Выводы. При проведении дифференциального диагноза кистозных изменений в плаценте, выявленных при УЗИ, следует помнить о редкой патологии – плацентарной мезенхимальной дисплазии, при отсутствии высокоскоростных сигналов кровотока внутри очага и нормально сформированном плоде. Необходима тщательная оценка анатомии плода, динамики роста плода и функционального состояния фетоплацентарного комплекса для раннего выявления осложнений и предотвращения ненужного прерывания беременности или досрочного родоразрешения.